登录方式
方式一:
PC端网页:www.rccrc.cn
输入账号密码登录,可将此网址收藏并保存密码方便下次登录
方式二:
手机端网页:www.rccrc.cn
输入账号密码登录,可将此网址添加至手机桌面并保存密码方便下次登录
方式三:
【重症肺言】微信公众号
输入账号密码登录
注:账号具有唯一性,即同一个账号不能在两个地方同时登录。
重症肺炎是临床常见病,但重症肺炎对呼吸科大夫而言仍然是很大的挑战。目前胸部影像学是诊断肺炎的金标准,但单纯通过影像学特征无法鉴别肺炎的致病原,甚至无法判断是否为感染因素所致的肺炎,因此导致治疗失败。需要住院治疗的社区获得性肺炎病人的治疗失败率6%~15%,需ICU治疗的重症肺炎治疗失败率甚至高达40%[1,2]。一旦治疗失败需要对病史、症状体征、影像学和病原学的更细致的回顾和分析。
临床资料
患者,女,61岁。主因“双下肢皮疹2月,咳嗽、发热2周”于2012年8月23日入院。患者2月前无明显诱因出现双下肢紫癜样皮疹,压之不退色,不伴疼痛、瘙痒,体温正常,无腹痛、腹泻、关节疼痛等不适,就诊于皮肤科,右下肢皮肤活检提示“白细胞破碎型血管炎”,予外用药物(具体不详)治疗,自觉皮疹逐渐减少。2周前患者无诱因出现发热,体温最高37.8℃,无寒战,伴咳嗽、咳黄痰,痰粘稠、不易咳出,伴食欲下降、恶心、腹痛、腹泻,排便最多9次/天,为水样便。5天来患者症状加重,体温升高入院。患者自发病以来,无口干、眼干、光过敏、脱发、口腔溃疡、雷诺现象、视力减退等症状,精神尚可,饮食较差,睡眠差,无尿频、尿急、尿痛等不适,尿量较前无明显变化、无泡沫,体重下降约2kg。既往类风湿关节炎23年,间断雷公藤2片治疗。否认结核病史,否认外伤史,否认烟酒等不良嗜好。否认家族中自身免疫性疾病病史及家族遗传病史。
入院检体
T 38.5℃,P 110次/分,RR 30次/分,BP 130/70mmHg;神志清楚,轮椅推入病房,营养欠佳;双下肢可见散在紫癜样皮疹,未见出血点,全身浅表淋巴结不大;双肺呼吸音叩清音,双肺呼吸音对称,双肺可闻及湿啰音;心率110次/分,心律齐, A2>P2,各瓣膜听诊区未闻及杂音;腹部平坦,腹软,左下腹、右下腹及剑突下压痛,无反跳痛及肌紧张,肝脾肋下未触及,双肾区无叩痛,移动性浊音(-),肠鸣音低,2次/分,未闻及血管杂音;右手示指和中指可见“天鹅颈”样改变,右腕活动受限,双膝关节肿胀,无明显压痛。双下肢轻度对称性可凹性水肿。
入院时辅助检查
入院查血常规:WBC 2.04*109/L、NE 79.7%、Hb 84g/L、PLT 48*109/L,ESR 8mm/h,PCT 0.31ng/ml。生化:Crea 88.6umol/L,Urea 9.34mmol/L,AST34IU/L,ALT24IU/L,ALB 22.9g/L,LDH 375IU/L。尿常规:蛋白(++)、RBC>100/Hp、80%变性红细胞。胸片提示双肺渗出(图6-1);
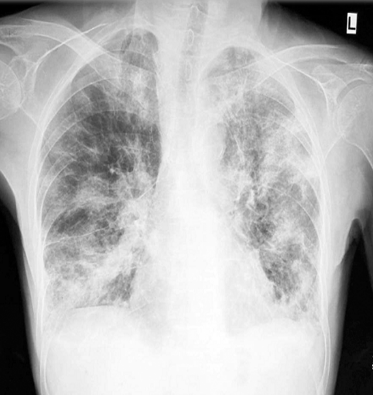
图6-1 入院时胸片:双肺多发片状渗出影,双侧肋膈角钝
胸部CT(图6-2)示双肺多发实变,以胸膜下为著,考虑感染性病变、不除外机化性肺炎,双侧胸腔积液。腹部B超提示双肾弥漫性病变、腹腔积液。痰培养(-),G试验、GM试验及隐球菌抗原(-),CMV+EBV+甲型流感病毒+乙型流感病毒IgM(-),CMV-DNA(-),多次痰找抗酸杆菌(-),T-SPOT-BT(-)。自身抗体ANA 1:100000、抗dsDNA抗体(IIF法)>1:800 (ELISA法)>800 IU/ml、抗rRNP抗体阳性、抗SS-A抗体阳性、P-ANCA阳性、C3 0.06g/L、C4<0.02g/L,RF 263 IU/ml。
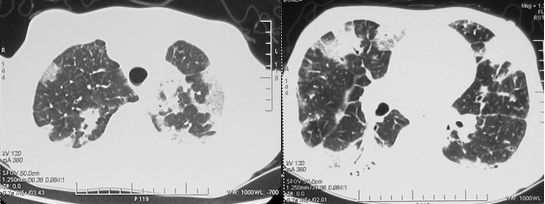
图6-2 入院时胸部CT:双肺多发实变,以胸膜下为著,考虑感染性病变,不除外机化性肺炎,双侧胸腔积液。
诊断社区获得性肺炎,系统性红斑狼疮,狼疮肾炎。患者及家属拒绝有创检查。经验性给予头孢哌酮/舒巴坦+莫西沙星抗感染治疗。患者呼吸困难进行性加重,出现少尿(300-400ml/d),肌酐升高,下肢水肿进行性加重,BNP升高,抗感染1周复查胸片提示双肺渗出较前明显增多(图6-3);
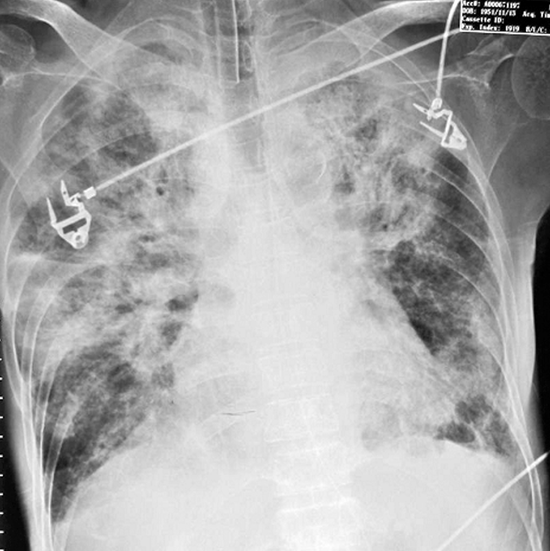
图6-3 抗生素治疗1周胸片:床旁卧位胸片,气管插管,左下肺野渗出影较前减少,右上肺野渗出影较前增多,双侧肋膈角较前锐利。
血气分析(面罩吸氧14L/min):pH 7.230,pCO2 41.4mmHg,pO2 56.9mmHg,sO2 83.3%,Lac2.4mmol/L;Hb降低为59g/L,遂转入呼吸重症监护室,并行气管插管,机械通气。同日行支气管镜检查,气管镜下未见明显异常,于左舌叶行支气管肺泡灌洗,回收液体为血性,灌洗过程中,颜色逐步加深,灌洗液细胞分类 巨噬细胞 11%、中性粒细胞 89%、含铁血黄素细胞 8%。BALF培养提示屎肠球菌,涂片找抗酸杆菌(-)、涂片找真菌(-)、PCP(-)、GM试验(-)、CMV-DNA < 500 copies/ml。考虑患者存在系统系红斑狼疮、弥漫性肺泡出血、急性肾损伤。更改抗生素为美罗培南+他格适,给予甲强龙500mg每日,连续3天冲击治疗,后减量为甲强龙 80mg/d,并予丙种球蛋白20g×3天治疗,持续床旁血液滤过。患者一般情况明显好转,体温下降,波动于37.0-37.5℃,腹泻好转,呼吸衰竭好转,尿量较前恢复(800-1000ml/d);复查ANA1:1000、抗dsDNA抗体(IIF法)1:100 (ELISA法)120 IU/ml,胸片提示渗出明显减少,机械通气1周撤机拔管。1周后患者体温再次明显升高(波动于38.0-39.0℃),伴咳黄痰,呼吸困难加重。复查胸部CT示左气胸,右肺脓肿(图6-4)。
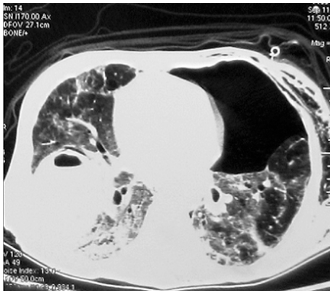
图6-4 入院3周CT:左侧气胸,皮下气肿,可见引流胸管,右肺脓肿,壁厚,内壁光滑,可见液平。纵隔向右移位。
予左侧胸腔闭式引流,抗生素调整为头孢吡肟+利奈唑胺。患者呼吸衰竭仍进行性加重,再次行气管插管,机械通气。支气管镜检查,行右中叶支气管肺泡灌洗,回收液为血性,颜色逐步加深,灌洗液细胞分类:巨噬细胞 21%、中性粒细胞 79%、含铁血黄素细胞 17%。PCP(-)、灌洗液培养提示产超广谱β-内酰胺酶大肠埃希菌,涂片找抗酸杆菌(+),涂片找真菌(-)、GM试验1.277,CMV-DNA 6.52×104 copies/ml。血培养阴性,血浆CMV-DNA:5.14×102 copies/ml,GM试验 0.712,PCT 2.71ng/ml,CRP 99.6mg/L。ANA1:1000、抗dsDNA抗体(IIF法)1:800 (ELISA法)457 IU/ml。肺脓肿穿刺引流,脓液为血性粘稠,常规:细胞总数286万/mm3,有核细胞18万/mm3,单核细胞40%,多核细胞60%;生化:TP 221.4g/L,ALB 58.6g/L,glu13.67mmol/L,LDH 16340IU/L,ADA 78.8U/L。支气管抽吸液培养:产超广谱β-内酰胺酶大肠埃希菌,真菌(-)。局部注射丁胺卡那霉素(0.1g+0.9%盐水50ml)。考虑患者存在肺部混合感染,抗生素调整为美平抗细菌、异烟肼+利福喷丁+拜复乐抗结核、卡泊芬净抗真菌治疗。肺脓肿引流液逐渐清亮,但患者的仍然持续高热,逐渐出现休克,双肺渗出增多,呼吸衰竭持续,CRP升至135mg/L。一方面考虑患者系统性红斑狼疮仍活动,但合并严重混合感染,激素冲击及加量风险大,给予血浆置换(共6次),丙种球蛋白,将甲强龙2周内由60mgQd逐渐减量至40mgQd,另一方面考虑可能和CMV感染或其它感染有关,加用稳可信、更昔洛韦治疗后,患者一般情况再次好转,患者的体温逐渐恢复正常,CRP将至30.5 mg/L,呼吸衰竭逐渐好转。复查ANA1:1000、抗dsDNA抗体(IIF法)1:100 (ELISA法)251 IU/ml。考虑系统性红斑狼疮相对稳定,故甲强龙逐渐减量,每2周减4mg至24mg。监测左侧气胸逐渐吸收,右侧胸腔引流量逐渐较少,引流液清亮,于引流2周后拔除双侧胸腔引流管。复查胸部CT平扫(图6-5)提示左侧气胸完全吸收,右中叶实变明显吸收。机械通气52天脱机拔管,转入风湿免疫科进一步治疗。
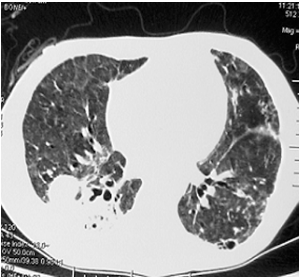
图6-5 入院6周CT:左侧气胸吸收,右侧肺脓肿较前缩小,原有双肺实变影大部分吸收。
讨论
本患者因发热、肺部渗出阴影为首发症状,符合肺炎的诊断标准:有新近出现的咳嗽、咳痰;发热;胸部X线示新发的肺部渗出影。肺炎诊断明确[3]。该患者的发病地点在医院外,故诊断社区获得性肺炎。需要有创机械通气(主要标准),且呼吸频率≥30 次/min,属于重症肺炎[3],同时伴有腹部症状、三系减少、肾脏损害等多器官系统受累。因此经验性抗生素治疗需覆盖非典型致病菌,尤其是军团菌。给予患者经验性头孢哌酮/舒巴坦+莫西沙星抗感染1周,患者症状不缓解,呼吸困难逐渐加重,需要调整治疗。在此期间所进行的病原微生物相关检查均未见阳性发现,因此需警惕非感染性肺炎。许多非感染性疾病可以出现呼吸道症状及肺部浸润影和系统性炎症反应的症状,易与感染性肺炎相混淆。且患者有类风湿关节炎病史。进一步检查显示ANA、抗dsDNA阳性,结合患者的多器官受累表现,根据目前新的SLICC的SLE诊断标准[4],患者存在浆膜炎(双侧胸腔积液)、肾脏改变、血液学改变(WBC<4×109/L、PLT<100×109/L),ANA、抗dsDNA阳性、补体降低,SLE诊断明确。系统性红斑狼疮是自身免疫介导的以免疫性炎症为突出表现的弥漫性结缔组织病。主要临床特征为血清中出现以抗核抗体为代表的多种自身抗体和多系统累,好发于育龄女性。此患者虽然年纪较大,但有结缔组织病史,也需要关注。
系统性红斑狼疮病人出现发热和肺部浸润阴影,鉴别诊断思路改变。SLE可以有肺部受累,多表现为胸膜炎,肺实质浸润的放射学特征是阴影分布较广、易变,与同等程度 X 线表现的感染性肺炎相比,SLE 肺损害的咳嗽症状相对较轻,痰量较少。SLE合并弥漫性肺泡出血死亡率高。SLE还可出现肺动脉高压、肺梗塞。鉴别SLE肺部浸润时,感染是最需要鉴别的疾病,决定着进一步的治疗方向。许多间接的依据提示 SLE 可能与某些感染因素,尤其是病毒感染有关,感染可以诱发疾病活动[5,6]。该患者的肺部渗出影是单纯狼疮所致?还是存在特殊感染?还是在感染基础上的狼疮活动?此时使用介入操作手段获得下呼吸道标本尤为重要。因此在病人气管插管机械通气第一天即进行了支气管镜检查并进行支气管肺泡灌洗。
患者支气管肺泡灌洗液呈血性,且随着灌洗的进行,回收液血性成分逐管增多,而非稀释减少,该患者虽存在血小板减少,但没有全身出血倾向,因此考虑符合肺泡出血的诊断。因患者呼吸衰竭重,未行多部位灌洗,结合CT表现,可诊断弥漫性肺泡出血。弥漫性肺泡出血为SLE严重的临床表现。由于有出血的影响,无法根据肺泡灌洗液中的细胞比例判断疾病的活动性。BALF还可以进行全面微生物学检测,较大限度避免上呼吸道污染,并且获得肺泡标本。
患者存在弥漫肺泡出血、急性肾功能不全,均为需要激素冲击治疗的SLE的重症表现。在肺泡灌洗液涂片细菌、抗酸杆菌阴性的条件下,开始激素冲击治疗,并给予丙种球蛋白。随后的病原学的检查也未见阳性结果。患者呼吸衰竭好转,尿量增加。从治疗反应可以证实,对患者的治疗是有效的,患者此时的肺部渗出影主要由于SLE炎症反应和弥漫性肺泡出血所致。而在病人好转,激素逐渐减量的过程中,患者再次出现发热,CT发现左气胸和右肺脓肿。可以推断患者在疾病早期的肺部浸润影除弥漫肺泡出血外,确有细菌感染的因素。在激素冲击治疗过程中,感染加重,形成肺脓肿,肺组织破坏形成气胸。支气管肺泡灌洗液仍为血性。此时血性的肺泡灌洗液可能来源于SLE的免疫损伤,也可能由于严重肺部感染、组织破坏,表现为血性。此时抗感染和激素治疗相互矛盾。为了减小治疗对患者免疫功能的抑制,此时选择进行血浆置换,并逐渐减量糖皮质激素,局部引流,加上全身抗感染药物的应用。虽然我们已知免疫抑制病人容易出现混合感染,尤其是条件致病菌的感染,但此患者的混合感染还是出乎意料,此时支气管肺泡灌洗液又起到了非常关键的作用。肺泡灌洗液结果证实,此患者的肺部感染的病原微生物为产超广谱酶的细菌、真菌、结核菌和CMV病毒的混合感染。有针对治疗后患者才逐渐好转。
随着糖皮质激素等免疫抑制剂的广泛使用,免疫抑制患者近年来呈不断增加趋势,而肺部感染作为免疫抑制患者最常见的感染性疾病,具有极高的病死率[7]。根据既往研究,免疫抑制患者合并肺部阴影的病因中,感染性因素约占70%,而非感染因素约占30%[8]。引起免疫抑制患者肺部感染的致病菌种类非常也多,包括细菌、真菌、病毒、非典型致病菌等,且往往为混合感染。真菌中以曲霉菌、隐球菌及念珠菌最为常见,且真菌感染致死率非常高。细菌感染中,则以耐药的葡萄球菌及革兰阴性菌更为多见。病毒感染中,巨细胞病毒肺炎最常见最具致死性,有报道称其病死率可高达84%[9],同时流感病毒、副流感病毒、腺病毒等也为肺部感染常见病原体。此外,结核分枝杆菌、伊氏肺孢子菌等特殊病原体在免疫抑制患者中也更为常见。免疫抑制患者肺部感染的另一个重要特点是影像学改变缺乏特异性,需积极与其他非感染因素鉴别,在初始经验性抗感染治疗无效的情况下,应积极行有创性检查,如肺泡灌洗等以获得病原学及其他病因证据,进行针对性治疗。
本例患者发病初期和治疗过程中正反复出现发热,肺部渗出影不断变化,支气管镜下表现类似,支气管肺泡灌洗均可诊断肺泡出血,但在疾病治疗的不同阶段,鉴别诊断的思路不同。虽然患者肺部改变均是免疫疾病和感染疾病共同的结果,但所占比重和治疗重点有在治疗中互相转化。需要细致综合分析。
重症肺炎是重症监护室常见疾病,原因复杂,对临床医生是很大的挑战。需要依靠临床医生综合分析病史、流行病学史、体格检查、实验室检查、影像学特征和治疗经过,进行相应的鉴别诊断,适时进行有创检查。这将会使患者获得早期的诊断并更早获得有针对性的治疗,改善患者预后。
 后可发表评论
后可发表评论




友情链接
联系我们
 公众号
公众号
 客服微信
客服微信