登录方式
方式一:
PC端网页:www.rccrc.cn
输入账号密码登录,可将此网址收藏并保存密码方便下次登录
方式二:
手机端网页:www.rccrc.cn
输入账号密码登录,可将此网址添加至手机桌面并保存密码方便下次登录
方式三:
【重症肺言】微信公众号
输入账号密码登录
注:账号具有唯一性,即同一个账号不能在两个地方同时登录。
作者:于鲲遥
单位:北京大学第一医院呼吸和危重症医学科
一次正压通气是如何发生的?
当我们进行一次正压通气时,需要给一个驱动的压力才能将气体送入肺内,这其中包含了几部分,首先是驱动压,包括外源性的正压和患者自主呼吸时膈肌下移产生的负压。需要克服的力包括,①阻力:主要涉及气道的阻力和送气的流速,这也是将气体送入肺中产生的力;②弹性阻力:简单理解为维持肺开放在一定容积下需要克服的力,主要涉及容量和顺应性。③内源性PEEP(PEEPi)。
通过上述公式可以看到,呼吸力学监测的主要指标包括压力、容量、流速和顺应性。
主要分为气道压(Paw)和食道压(Pes),Paw包括气道峰压(Ppeak)、气道平台压(Pplat)、内源性PEEP(PEEPi)及P0.1。在临床工作中,我们希望了解患者更多的病生理特性,也会测量其他压力,胸腔内负压可能是我们最关注的,可以通过Pes进行测量。
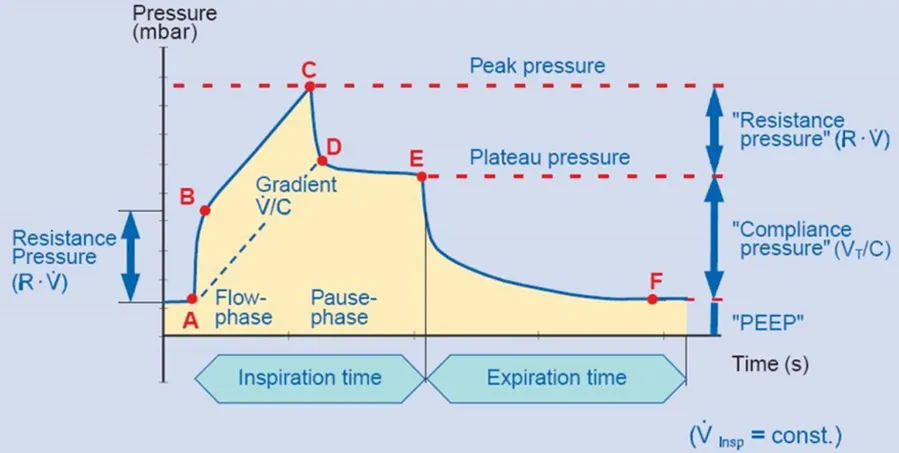
(1)Paw:上图是在一次定容通气下的压力-时间曲线,曲线中有几个压力节点,例如,C位置是Ppeak,即在进行一次定容通气时能达到的最大压力,可反映克服气道阻力与使肺泡容积增加所需要的整体压力的大小。
(2)Pplat:上图从D点到E点是吸气后的暂停状态,此时依然会需要一个比较高的压力,我们称之为“平台压(Pplat)”,它是维持肺泡开放的压力,所以与肺顺应性和容量有关。
由以上两点我们可以得知,在定容通气未改变容量的情况下,如果患者出现了气道压力的升高,表现为单纯的Ppeak升高,而不伴有Pplat升高时,往往提示患者气道阻力升高。如果患者出现了单纯Pplat的升高,提示患者肺顺应性下降。
(3)PEEPi:如果患者PEEPi升高,提示可能出现肺动态过度充气或者存在气体陷闭。
测定方法:①气道阻断法:气道阻断法测量PEEPi和Pplat时,要求患者是在没有自主呼吸的状态下,用容控通气、方波流速。如果在吸气末阻断通气,会导致吸气末暂停,此时的压力即为Pplat。如果在呼气末阻断通气,持续5~8 s,此时的压力为PEEPi。②食道测压法:可以在患者有自主呼吸的情况下进行测定吸气流量始动点食道内压,相当于是呼气末结束时的压力,我们认为是PEEPi。但有时可能会受到一些负压的影响,需要同步测量胃内压(Pga)来进行校正,才能得到较为准确的PEEPi。
(4)P0.1:P0.1是在吸气开始前0.1秒内的气道闭合压,其反映的是患者自主呼吸努力的程度。在正常生理状态下,P0.1为0.5~1.5 cmH2O。在机械通气情况下,P0.1约为3.5 cmH2O[1]。P0.1的升高往往与患者自主呼吸能力增强有关,即使是在ECMO辅助下,这样的线性关系依然存在[2]。
图源:Intensive Care Med, 2018, 44(9):1532-1535.
图源:Anesthesiology, 2016, 125(1):159-167.
(5)Pes:Pes可以间接反映胸腔内压,其测量方法相对简单,将Pes测量导管送入食道内,固定到相对准确的位置,然后进行读数即可。先将测量导管送入胃内,然后再回撤,当可以看到心脏搏动时(心脏搏动产生压力),则认为位置较理想。Pes测定出来后,可以进行其他指标的测评,例如,胸腔内压(Ppl)和Paw之差即可得到跨肺压(PL),这是与肺损伤相关的指标,另外,胃内压(Pga)和胸腔内压(Ppl)之间进行运算,可以得出跨膈压(Pmus),能够帮助判断患者的自主呼吸努力。
容量涉及潮气量(VT)、分钟通气量(MV)、生理无效腔和呼气末肺容量(EELV),其中最常用的是VT和MV。在呼吸机上,根据流速和时间的积分,可以得到VT,VT与呼吸频率的乘积即为MV。生理无效腔和EELV的测定可能需要用到其他方法。
流速主要涉及吸气流速和呼气流速,临床上流速多与人机不同步有关。此处不作赘述。
顺应性包括静态顺应性和动态顺应性。
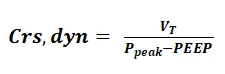
实际上,阻力并不是一个力,它反映的是在一定的驱动压下产生气流的情况,这种气流在不同状态下是不一样的。最理想的状态是层流,但层流在现实生活中很难观测到,有时我们也会认为小气道中气体流动类似层流,气管内气流类似湍流,根据流体力学公式,我们可以得知,克服气道阻力所需要的驱动压力,与流速成正比,与气道管径成反比。
层流:
时间常数是测定气体在肺组织分布和排空的时间,反映的是肺组织对压力变化反应的速度,正常值约为0.4。
综上,可以将呼吸力学监测指标分为可观测的指标(压力、容量、流速、P-V曲线)和可计算的指标(阻力、顺应性、跨肺压、跨膈压、无效腔、呼吸功),通过这些指标,我们要分析患者究竟是怎样的病生理过程。例如,患者气道阻力上升,提示可能存在气道阻塞,或者人工气道中形成痰痂,或者出现气道痉挛;如果顺应性发生改变,则考虑是否为间质病变加重,或者出现胸腔积液/气胸等影响呼吸系统整体顺应性的情况;如果跨肺压变化,需要警惕出现呼吸机相关肺损伤,而跨膈压、PEEPi等与有无呼吸肌疲劳、动态过度充气以及人机不同步相关。
呼吸力学的应用领域主要包括:调整呼吸支持水平,评估肺脏功能,避免肺脏损伤,指导撤机,评价人机协调。
Pes用于ARDS患者PEEP滴定。在2008年N Engl J Med发表了一篇文章,该研究将患者分为两组,一组患者通过监测Pes滴定PEEP(Pes滴定组),目标是将跨肺压控制在一定范围内,另一组使用ARDSnet法(对照组),经验性PEEP-FiO2滴定PEEP,经过一段时间机械通气发现,Pes监测组患者PEEP的患者有更高的PEEP,但其氧合指数和肺顺应性更好,而两组的跨肺压水平却近似,该组患者的28天死亡率低于对照组,但并无统计学差异[3]。2019年JAMA上发表了一篇类似研究,同样是一组患者用Pes滴定PEEP,另外一组用经验性PEEP-FiO2滴定PEEP,结果发现两组各项指标之间均无显著性差异。但该研究使用的经验性PEEP-FiO2实际上选择的是高PEEP[4]。
综合上述两项研究,在得到公认的经验性的PEEP和FiO2之前,在人种差异、病情差异等都存在的情况下,是否意味着通过Pes滴定PEEP能够得到一个优于或者不弱于经验性调节的PEEP值,从这方面来讲,有一定的积极意义。
P0.1与患者自主呼吸努力的相关性,可作为调整呼吸支持的参考。既往研究发现,P0.1下降于PEEPi的下降存在一定关系[5],通过P0.1下降预测患者PEEPi的下降,其灵敏度和特异度可以达到71%和88%,而调整呼吸支持后,P0.1下降提示患者呼吸功的下降,其灵敏度和特异度可以达到到86%和91%[6]。所以,如果评价呼吸支持的调整是否合适时,可以通过观察P0.1的变化来判断,可以纳入常规诊疗流程。
自主呼吸会在胸腔内产生一个正压或者负压,而它与气道压综合作用产生的跨肺压,才是真正与肺损伤有关的压力。所以通过Pes测定来评价患者的跨肺压,间接反映患者肺损伤情况,这是呼吸力学监测用于避免肺损伤非常经典的应用场景。
呼吸力学监测用于避免肺损伤,在自主呼吸患者中也能发挥这种作用。自主呼吸患者也会出现肺损伤,这在早期可能并未被充分认识,但现在支持呼吸相关肺损伤越来越受到重视,分为肺脏损伤和膈肌损伤。肺脏损伤主要是过高的呼吸努力,包括人机不同步、PEEP过低导致肺不张,以及PEEP过高导致的过度充气,这些情况都可以通过上述呼吸力学指标进行评价。膈肌损伤与容控通气引起的向心性收缩,人机不同步引起的无效触发及反向触发,过度呼吸支持可导致废用性问题等。上述情况通过呼吸力学监测也能识别出来。对于支持通气下的肺损伤,利用呼吸力学工具也可以观测到。
2005年发表的一项研究显示,通过Pes的变化趋势来预测撤机失败较浅快呼吸指数有一定优势,但这种优势并无统计学差异。在自主呼吸试验期间,持续监测Pes波动为患者管理提供了一定的指导,但并不是用于决定何时开始撤机的测试[7]。P0.1也可以用来进行指导撤机。有研究表明,撤机失败组的P0.1显著高于撤机成功组,这种差异具有统计学意义,这提示在自主呼吸试验时,该组患者的吸气能力更强,呼吸窘迫可能更严重,但该研究并未发现能够预测撤机成功的良好cut off值,提示P0.1存在不同个体差异,再同一患者P0.1的变化比其绝对值本身,对于预测撤机失败可能更有意义[8]。
一些进展
随着医学的进步和研究的进展,呼吸力学监测的角度在不断变化。在早期,肺损伤被认为是“容积伤”,之后更多认为是“压力伤”,而新近的研究提出肺损伤可能是“能量伤”[9],这种演变或许会使未来监测指标更加细化。
呼吸力学监测给临床带来很大帮助,但参数过多有时也会给临床带来困惑,如果彼此之间提供了相反的意见,很难进行判断。虽然多参数判断对临床医生来说是弱项,但却是计算机判断的强项,随着人工智能的发展,它对临床大量参数的整合和辅助临床判断或许会有所帮助。2021年发表的一篇文献作者建立了利用人工智能建立的基于多种临床参数的危重症患者模型,但该研究与很多基于人工智能的研究类似,其模型的可解释性依然较差,临床医生无法获知各项指标所发挥的实际作用,因此也难以从中获得干预措施的提示。此外,该难以在其他中心对该结果进行复现 ,临床普适问题依然无法解决[10]。但随着相关算法的不断更新,在一些研究中已经可以看到纳入指标对于决策所占的权重。未来我们或许能够看到一个基于人工智能的呼吸力学监测集束化的评估流程。此外,人工智能常用于人机不同步的识别与干预,2012年发表的一篇文献利用Better Care®系统识别无效触发,帮助临床医生更好地识别患者的人机不协调[11]。近年来类似的研究颇多,这也是未来发展的方向。
呼吸力学监测是探寻病生理改变本源的工具,也是孕育呼吸治疗新方法的摇篮。对于初学者,呼吸力学监测像是读不懂的梦魇,但却是必须翻越的高山。
参考文献
[1] Telias I, Damiani F, Brochard L, et al. The airway occlusion pressure (P0.1) to monitor respiratory drive during mechanical ventilation: increasing awareness of a not-so-new problem[J]. Intensive Care Med, 2018, 44(9):1532-1535.
[2] Mauri T, Grasselli G, Suriano G, et al. Control of Respiratory Drive and Effort in Extracorporeal Membrane Oxygenation Patients Recovering from Severe Acute Respiratory Distress Syndrome[J]. Anesthesiology, 2016, 125(1):159-167.
[3] Talmor D, Sarge T, Malhotra A, et al. Mechanical ventilation guided by esophageal pressure in acute lung injury[J]. N Engl J Med, 2008, 359(20):2095-2104.
[4] BeitlerJ R, Sarge T, Banner-Goodspeed V M, et al. Effect of Titrating Positive End-Expiratory Pressure (PEEP) With an Esophageal Pressure-Guided Strategy vs an Empirical High PEEP-Fio2 Strategy on Death and Days Free From Mechanical Ventilation Among Patients With Acute Respiratory Distress Syndrome: A Randomized Clinical Trial[J]. JAMA, 2019, 321(9):846-857.
[5] Alberti A, Gallo F, Fongaro A, et al. P0.1 is a useful parameter in setting the level of pressure support ventilation[J]. Intensive Care Med,1995, 21(7):547-553.
[6]Mancebo J, Albaladejo P, Touchard D, et al. Airway occlusion pressure to titrate positive end-expiratory pressure in patients with dynamic hyperinflation[J]. Anesthesiology, 2000, 93(1):81-90.
[7] Jubran A, Grant B J, Laghi F, et al. Weaning prediction: esophageal pressure monitoring complements readiness testing[J]. Am J Respir Crit Care Med, 2005, 171(11):1252-1259.
[8] Fernandez R , Raurich J M, Mut T, et al. Extubation failure: diagnostic value of occlusion pressure (P0.1) and P0.1-derived parameters[J]. Intensive Care Med, 2004, 30(2):234-240.
[9] Marini J J, RoccoP R M, Gattinoni L, et al. Static and Dynamic Contributors to Ventilator-induced Lung Injury in Clinical Practice. Pressure, Energy, and Power[J]. Am J Respir Crit Care Med, 2020, 201(7):767-774.
[10] Mamandipoor B, Frutos-Vivar F, Peñuelas O, et al. Machine learning predicts mortality based on analysis of ventilation parameters of critically ill patients: multi-centre validation[J]. BMC Med Inform Decis Mak, 2021, 21(1):152.
[11] Blanch L, Sales B, Montanya J, et al. Validation of the Better Care® system to detect ineffective efforts during expiration in mechanically ventilated patients: a pilot study[J]. Intensive Care Med, 2012, 38(5):772-780.
作者简介
于鲲遥
*本文根据“呼吸危重症菁英秀”第五期专题视频整理,感谢于鲲遥医生予以审核。
 后可发表评论
后可发表评论




友情链接
联系我们
 公众号
公众号
 客服微信
客服微信