登录方式
方式一:
PC端网页:www.rccrc.cn
输入账号密码登录,可将此网址收藏并保存密码方便下次登录
方式二:
手机端网页:www.rccrc.cn
输入账号密码登录,可将此网址添加至手机桌面并保存密码方便下次登录
方式三:
【重症肺言】微信公众号
输入账号密码登录
注:账号具有唯一性,即同一个账号不能在两个地方同时登录。
作者:梁瀛
单位:北京大学第三医院呼吸与危重症医学科
休克是危重症领域最常见的急危重症之一,其核心是细胞与组织缺氧及灌注受损导致的循环衰竭。准确评估血流动力学状态、快速识别休克类型并指导治疗,是改善患者预后的关键。床旁超声作为一种无创、快速、可重复的工具,已成为血流动力学评估的利器。本文将系统梳理休克的类型、血流动力学评估技术,重点阐述床旁超声在各类休克中的应用特点与临床价值。
1. 休克的定义和分类
休克是血流动力学紊乱的终极表现,其定义为由于细胞/组织缺氧及灌注受损,不能满足当前代谢需要而导致的循环衰竭,进而导致脏器功能不全和不可逆的细胞损伤。所以,休克的治疗目标有两方面,一是改善细胞/组织缺氧,二是改善组织低灌注。
根据病因和表现,休克可分为四类:低血容量性休克,心源性休克,梗阻性休克,分布性休克(图1)。
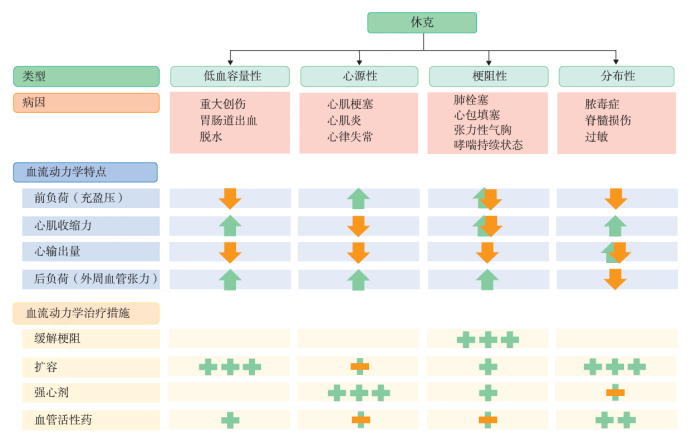
图1 休克的分类
2. 血流动力学的评估技术
评估血流动力学的技术可分为侵入性与非侵入性两类,临床需根据患者的病情权衡风险与获益:
(1)侵入性监测技术:包括肺动脉导管(Swan-Ganz导管)、脉搏指示连续心输出量监测(PiCCO)、动脉导管和中心静脉导管。此类技术虽为评估血流动力学的“金标准”,但因其风险较高、费用昂贵,需权衡利弊。
(2)非侵入性监测技术:包括床旁超声(肺部超声、心脏超声等)、生物阻抗法(NICOM)、光电体积描记术、微循环评估(舌下微循环、正交偏振光谱成像)等。
床旁超声在血流动力学评估中作用关键,具备快速、安全、有效的特性,是实用的床旁工具。其凭借独特的技术特点,可鉴别休克病因,为脓毒症患者补液提供液体治疗策略指导,还能监测治疗反应。
2024年J Clin Med 杂志发表的一篇文献展现了床旁超声鉴别休克分类的作用。研究按照心脏指数(CI)将患者分为两类,即低CI组[CI<2.2 L/(min・m²)]与高CI组[CI≥2.2 L/(min・m²)]。低CI组又分为三类:①梗阻性休克:含心包填塞、气胸、肺栓塞,超声可评估,如心包填塞需观察心包积液与吸气时右心室塌陷,气胸需观察是否存在“条形码征”或“平流层征”,肺栓塞观察是否存在右室超负荷、三尖瓣收缩期位移(TAPSE)改变或肺动脉高压等;②心源性休克:超声评估心脏收缩/舒张功能、充盈、瓣膜情况等,识别心肌、瓣膜病变;③低血容量性休克:监测下腔静脉宽度、呼吸变异度等指标及容量反应性。高CI组也分为三类:①动力性梗阻:常见肥厚性心肌病,超声可识别相关特征;②液体反应性与耐受性:借助超声指标评估,指导补液策略;③心室和血管偶联机制失衡:借助超声可评价左心室收缩末期弹性与动脉弹性,判断是否心室-血管偶联失衡。
1. 梗阻性休克
梗阻性休克是指血液循环的主要通道(心脏或大血管)受到机械性梗阻,造成回心血量或心排血量下降而引起的循环灌注不良、组织缺血缺氧。其主要的病理生理机制是由于内部或外部的梗阻因导致回心血量减少,左心室流出道受阻,引起心室排空/充盈受损,心室顺应性降,最终导致心输出量(CO)减少。
1.1 肺栓塞(急性肺心病)
肺栓塞会显著增加右心室后负荷,导致右心室扩张和功能障碍。与左心室相比,正常成人的右心室较小,且适应于低压、低阻力循环。然而,急性或慢性肺血管阻力升高会引发右心室衰竭。急性肺栓塞超声表现为右心室扩张(右心室/左心室比值≥1)、室间隔“D型”变形,伴随收缩末期室间隔运动异常(图2)。
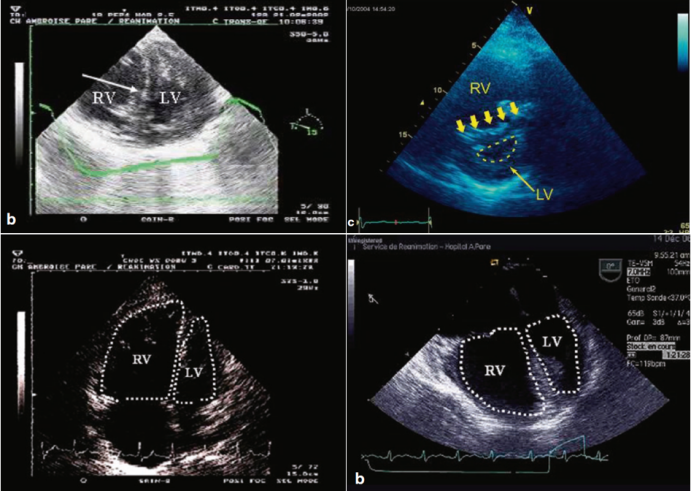
图2 肺栓塞肺超声表现
除了上述征象,肺栓塞(急性肺心病)还有其他超声表现:①三尖瓣环收缩期位移(TAPSE)缩小,静脉回流梯度减少(<16 mm,提示右室收缩功能降低)。TAPSE测量方法:M型超声,四腔心切面测量三尖瓣环从舒张末期到收缩末期的纵向位移(图3);正常值≥17 mm。②下腔静脉扩张且吸气时无塌陷(提示右心负荷过重)。③右心室腔内直接探及血栓(特异性高)。
对于肺栓塞而言,单一指标的敏感性较低,多种征象结合后可提高阳性预测值。
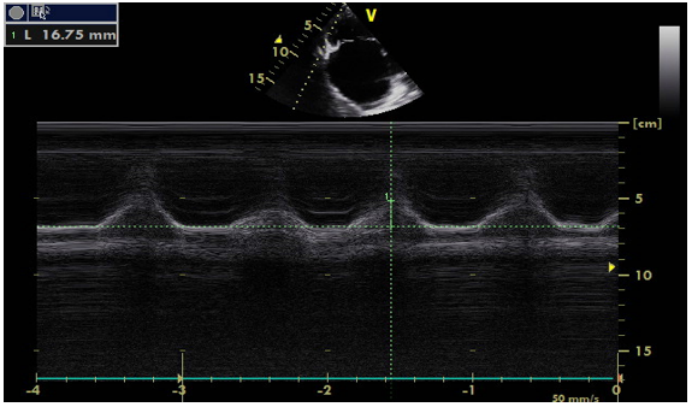
图3 TAPSE测量方法
1.2 心包积液
超声检测心包积液的能力取决于积液的大小和在不同超声视窗的分布,较大的积液导致心脏周围可见的无回声空间。通过长轴切面,可以检测到少量后心包积液;通过心尖四腔切面,可以评估右心房、右心室游离壁的运动(图4)。
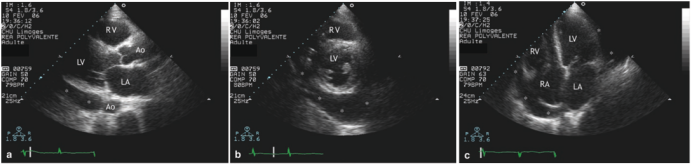
图4 心包积液的超声检测(*区域为心包积液)
心脏压塞的超声诊断:包括右心腔在吸气时增大的比例下降、右心房收缩期塌陷、右心室游离壁在舒张期塌陷、下腔静脉内径增宽呼吸变化率减低(视频1,图5)。右心房的收缩期塌陷是早期心脏压塞的一个敏感标志,早期阶段敏感性为50%,晚期阶段敏感性可达100%。然而,在右心室充盈压力升高的患者中,如由肺动脉高压或高血容量引起,跨膜压力可能需要更高才能导致心房塌陷,从而降低压缩效应。
视频1 心脏在心包腔内活动度增加(Swinging heart pattern)
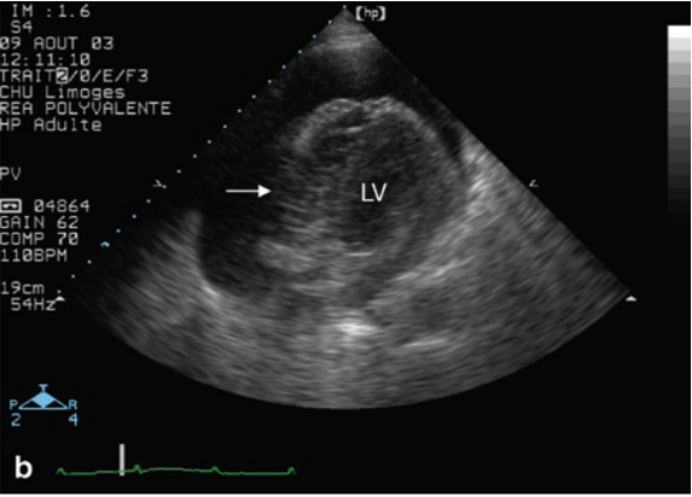
图5 右心室在吸气时塌陷
此外,还有一些特殊情况,例如:外科术后出现心包内血肿、纵隔血肿,心包粘连、肿瘤,都可能导致超声图像不典型,需要经食道超声辅助(图6,图7)。
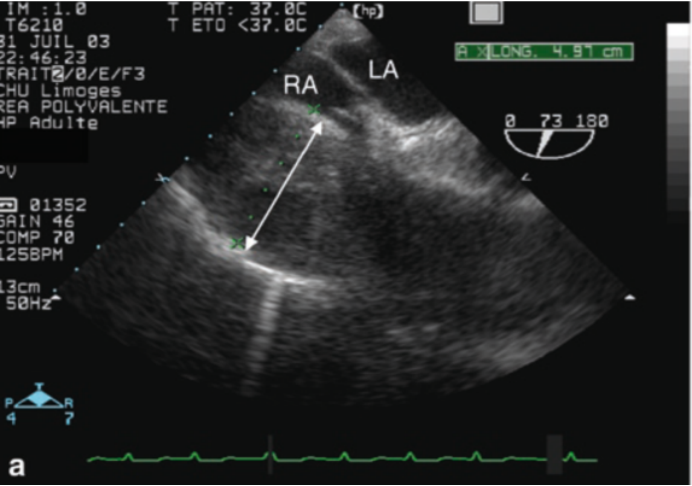
图6 经食道超声显示心包内巨大血肿
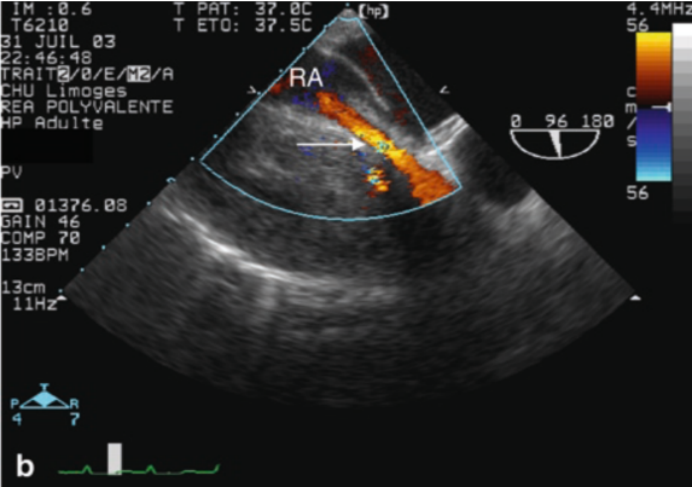
图7 右心房被血肿压迫,血流信号减少
心包积液与胸腔积液的鉴别在临床中也存在一定困难, 一般我们在胸骨旁长轴进行鉴别: 胸腔积液的无回声区可延展至降主动脉后方, 且与心脏的结构关系并不密切; 心包积液通常在主动脉前方终止, 且与心脏的关系更为密切(图8)。
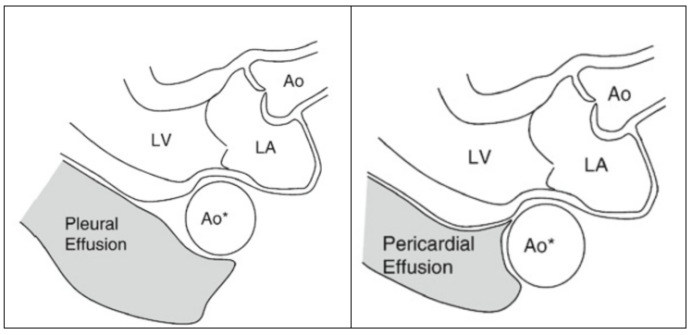
图8 胸腔积液与心包积液的鉴别
通过该患者多切面超声图像分析:①胸骨旁长轴切面(图9a):于后心包区域可见无回声区,需鉴别心包积液与胸腔积液。从解剖定位看,无回声区在主动脉(Ao)前方或外部。②左室短轴切面(图9b):无回声区显示更清晰,其位于左室后方,与心室壁贴合关系不紧密。③剑突下切面(图9c):未探及明显心包积液征象(心包腔内无特征性无回声区)。④肺部超声(图9d):胸腔内明确探及无回声区(*号标识的区域)。结合前序切面的定位分析,可印证胸骨旁长轴的无回声区为胸腔积液,而非心包积液。
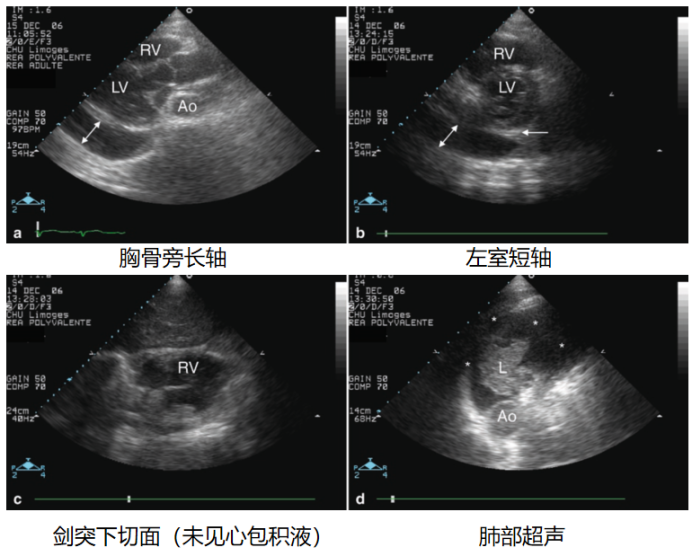
图9 心包积液与胸腔积液的超声鉴别
通过组织多普勒频谱分析也可以识别心包压塞。因为在生理状态下,左心室每搏量(SV)在吸气相轻微下降、呼气相轻微增加,右心室SV与之相反。正常情况下SV在吸气-呼气相差异较小;如果SV差异性增大,则提示心包压塞。在心包压塞的患者中,二尖瓣/三尖瓣流速在吸气相与呼气相差异度增大,表现为二尖瓣E波峰值流速在吸气时下降率≥25%;而跨三尖瓣流速增加≥40%。
如图10和图11所示:基于二尖瓣及三尖瓣血流频谱分析心包压塞的血流动力学特征:①二尖瓣血流频谱(图10):呼气相二尖瓣峰值流速约60 cm/s,吸气相降至约40 cm/s。二尖瓣峰值速度变异率=(60-40)/60×100%≈33%。当二尖瓣血流呼吸变异率>25%时,提示存在心包压塞。②三尖瓣血流频谱(图11):吸气相三尖瓣峰值流速约为80 cm/s,呼气相约为40 cm/s。三尖瓣峰值流速变异率=(80-40)/80×100%=50%。当三尖瓣流速增加≥40%,提示存在心包压塞。
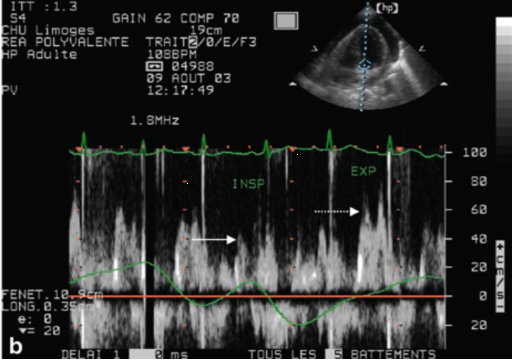
图10 二尖瓣血流频谱
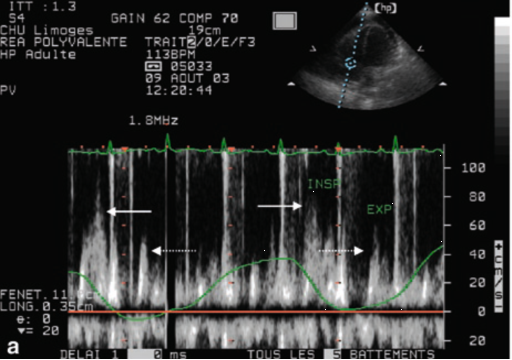
图11 三尖瓣血流频谱
1.3 气胸
床旁超声在气胸诊断中的敏感性为86%~98%,特异性为97%~100%。超声表现:①B模式:肺滑动征缺失,B线消失,阴性预测值高(99%~100%);②M模式:“平流层征”,其特点为超声图像上胸膜上下区域的水平线丧失运动,提示肺滑动缺失;③肺点征:可见正常肺滑动与静止胸膜线的交界点,该点随呼吸周期移动。肺点征是气胸的一个高度特异性征象。气胸发生后,胸腔内气体使脏层与壁层胸膜分离,局部肺滑动消失;而未被气体占据的区域仍可看到肺滑动。二者之间的边界即“肺点”,其位置随呼吸移动。
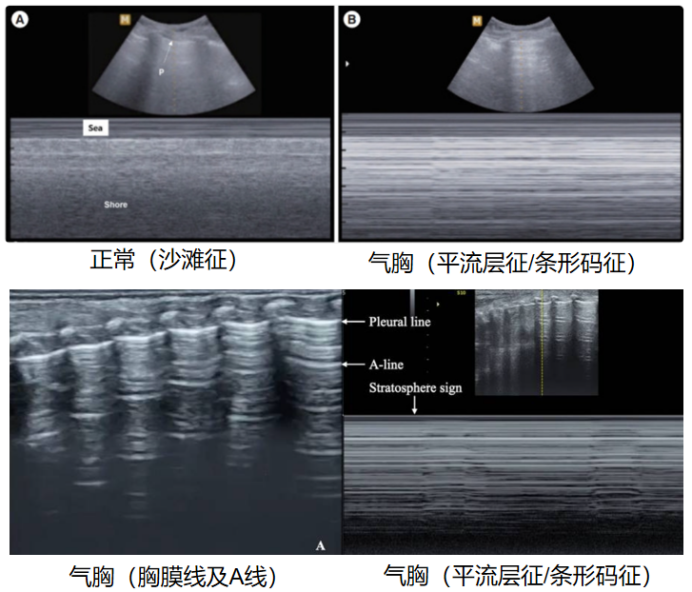
图12 气胸的超声征象
2. 心源性休克
在诊断心源性休克时,床旁超声是关键评估工具,主要针对左心室功能、充盈压(右心房压力、下腔静脉直径)及瓣膜功能展开评估。
2.1 左室收缩功能评估
(1)短轴缩短率(shortening fraction,SF):SF通过不同维度(直径或面积),反映左室短轴方向的收缩能力。有两种计算方法:①直径法(M超测量):取胸骨旁长轴切面,将M超探头置于乳头肌连接处,确保垂直于室间隔(图13)。计算公式:(舒张末期内径-收缩末期内径)/舒张末期内径。正常范围:24%~36%。②面积法(二维超声测量):取左室短轴切面,探头置于乳头肌连接处并垂直于室间隔,获取舒张末期与收缩末期左室短轴面积(图14)。计算公式:(舒张末期面积-收缩末期面积)/舒张末期面积。正常范围:38%~60%。
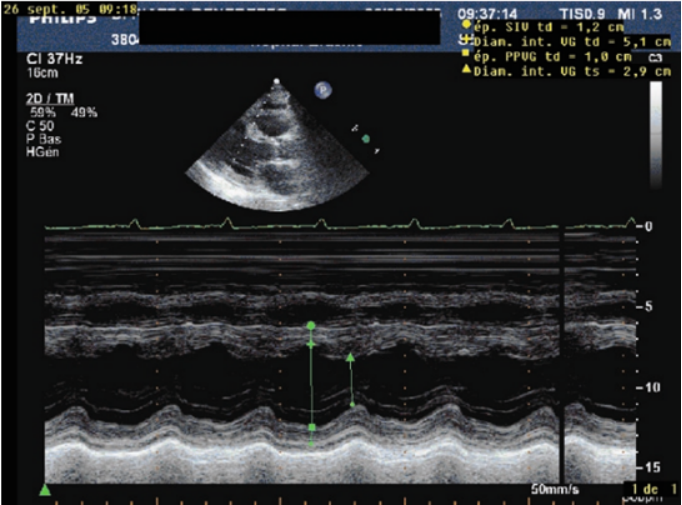
图13 直径法测量短轴缩短率
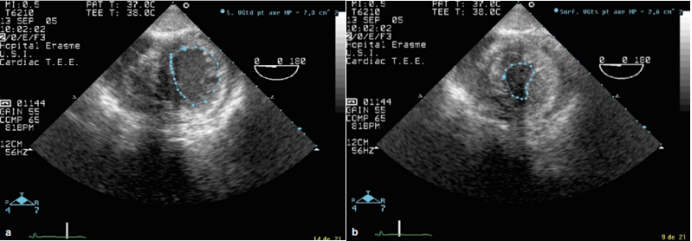
图14 面积法测量短轴缩短率
(2)左室射血分数(LVEF):Simpson法或面积长度法估算左室舒张末期容积和收缩末期容积,通过计算公式:(舒张末期容积-收缩末期容积)/舒张末期容积,得到的值即为LVEF(图15)。正常值为>60%。
图15 超声评估左室射血分数
2.2 充盈压的评估
(1)右房压:评估右房压时,常通过床旁超声测量下腔静脉直径及其塌陷性来估算。具体如下:需先以剑突下长轴切面为标准切面,清晰显示下腔静脉从右心房入口至肝静脉段,再借助M型超声捕捉下腔静脉随呼吸的动态变化以精准测量(图16)。测量呼气末直径(正常参考值1.5~2.5 cm,>2.5 cm提示容量过负荷),并计算塌陷率【公式:(最大直径-最小直径)/最大直径×100%】。若下腔静脉内径<1.0 cm且呼吸变化率>50%, 提示容量不足。结合下腔静脉直径与塌陷率分层判断右房压: ①当下腔静脉直径<2 cm时: 塌陷率>55%, 提示右房压为0~5 mmHg; 塌陷率30%~50%, 提示右房压为0~10 mmHg; 塌陷率<30%, 则无法估算右房压。②当下腔静脉直径>2 cm时: 塌陷率>55%, 右房压为0~10 mmHg; 塌陷率30%~50%, 右房压为10~15 mmHg; 塌陷率<30%, 右房压为10~20 mmHg。此方法利用下腔静脉呼吸变异特性, 通过超声精准测量与公式推导, 实现右房压的间接评估, 为心源性休克等场景下的容量状态、右心功能判断提供关键依据。
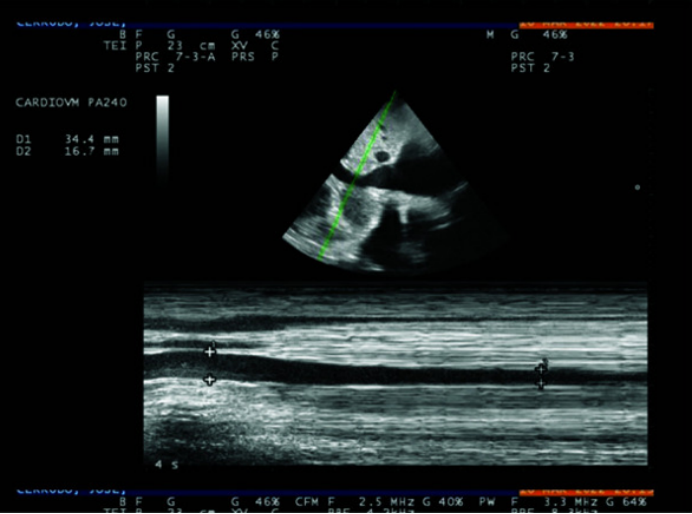
图16 M超测量下腔静脉直径
2.3 急性心肌梗死
视频2 左室长轴切面,左室基底部和中段运动减低
视频3 左室短轴切面,前段严重运动功能减退和心肌变薄
视频4 室间隔破裂
视频5 左心室游离壁破裂
2.4 瓣膜功能障碍
常规超声检查包括观察瓣膜增厚、钙化、赘生物或瓣膜活动受限,识别瓣膜的狭窄或反流。常见的瓣膜功能障碍有:①主动脉瓣狭窄:瓣叶开放狭窄的程度、是否存在钙化或硬化、瓣叶活动性;②主动脉瓣反流:左室流出道(LVOT)横截面与纵截面内反流喷射分布;③二尖瓣反流:左心房内喷射扩展及其分布情况;④二尖瓣狭窄:瓣叶钙化、硬化、活动受限以及舒张期反常后移现象。视窗显示不良、双心室功能障碍、重度瓣膜疾病或顽固性心源性休克情况下,需综合肺动脉导管或经食管超声心动图。
3. 分布性休克[CI≥2.2 L/(min·m2)]
分布性休克主要包括动力性梗阻(如肥厚性心肌病)及感染性休克。
3.1 动力性梗阻
动力性梗阻可发生于左室流出道(LVOT)或心室水平。其中,左室流出道梗阻的经典超声征象为收缩期二尖瓣前叶前移(SAM征);心室水平梗阻则由多种因素引发,包括低血容量、剧烈运动、左心室后负荷降低等情况。
左室流出道动力性梗阻的超声表现具有特征性:左室舒张末内径<4 cm,室间隔增厚,LVOT可探及湍流信号,SAM征;连续波频谱多普勒检测时,呈现高速、匕首状收缩期晚期高峰,且峰值压力梯度(PPG)≥30 mmHg。上述这些表现可作为诊断与评估的关键依据。
图17所示为SAM征,图中可见二尖瓣的后叶和前叶,心室收缩时,二尖瓣前叶凸向主动脉方向,导致这一区域的前向血流减少。此种情况下会出现二尖瓣相对性关闭不全,所以在左室收缩时,可以看到由左室向左房的反向血流。
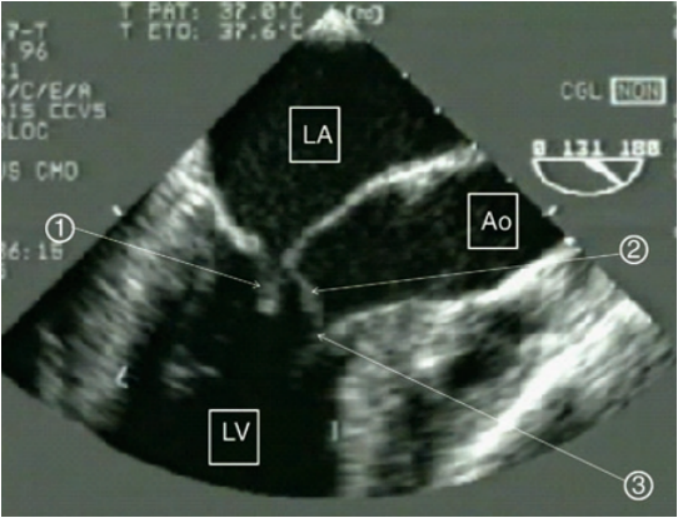
图17 SAM征
注:①为二尖瓣后叶;②为二尖瓣前叶;③为室间隔肥厚向LVOT突出。
3.2 容量反应性
在评估脓毒性休克或感染中毒症患者时,容量反应性是关键监测维度,核心聚焦于CO)与SV的动态变化。由于CO=SV×心率,直接计算需先获取SV,流程相对复杂,而速度时间积分(VTI)可作为SV的替代指标,这是因为LVOT横截面积与VTI乘积即为SV,借助VTI可间接反映SV。
结合临床实践,容量反应性的超声评估路径包括:补液试验后,若LVOT的VTI变异率>20%,提示容量反应性良好;此外,被动抬腿试验后CO增加>10%、LVOT收缩期峰值流速变异性>12%、下腔静脉呼吸变化率改变>18%、呼气末暂停15秒后心脏指数(CI)增加>5%,也可作为容量反应性的辅助判断依据。
补液复苏策略不仅基于液体负荷后CO增加的可能性(即容量反应性),还应考虑充血性心力衰竭的风险(液体耐受性),液体耐受性取决于液体推注后维持正常充盈压的能力。
通过超声监测多维度指标,判断心脏、肺脏、大静脉对液体的耐受阈值,核心指标包括:①肺动脉阻塞压(PAOP):E/e′>10时,可以间接反映PAOP增加,进而提示左室舒张末内压升高;②右心超负荷:出现室间隔D型征、室间隔矛盾运动,或右室/左室(RV/LV)面积比>1,提示右心容量负荷过重;③肺淤血:胸腔积液伴3个以上肺象限B线,提示肺间质水肿,液体已超过肺循环耐受;④大静脉淤血:VExUS-C评分≥1提示与肾灌注损伤的静脉淤血。
4. 脓毒性休克
针对脓毒性休克,国外学者提出规范化诊疗流程:脓毒症患者入院后,立即启动容量复苏,若存在低血压,同步给予去甲肾上腺素等血管活性药物。在此阶段,超声心动图需作为核心评估工具,分步骤指导治疗决策:①上腔静脉动态评估:测量上腔静脉直径随呼吸变化幅度(△SVC),若△SVC>36%,提示容量反应性良好,可继续扩容;若△SVC<36%,需进一步评估左室功能。②LVEF分层:若LVEF正常(>40%~45%):评估右室/左室面积比(RVA/LVA),若比值<0.6,仍可尝试扩容;若>0.6,提示右心负荷已较重,扩容需谨慎,需结合呼吸支持策略调整并优化血管活性药物剂量。若LVEF降低(<40%~45%):提示左心收缩功能障碍,应优先给予正性肌力药物,改善心肌收缩力。
5. RUSH方案
RUSH方案(Rapid Ultrasound in Shock)的核心是通过系统性的超声评估,快速识别休克的常见类型(如低血容量性、心源性、分布性、梗阻性),从而指导紧急处理。该方案遵循“泵-容量-脉管”三步评估逻辑,构建休克病因与血流动力学的快速诊断路径(图18)。
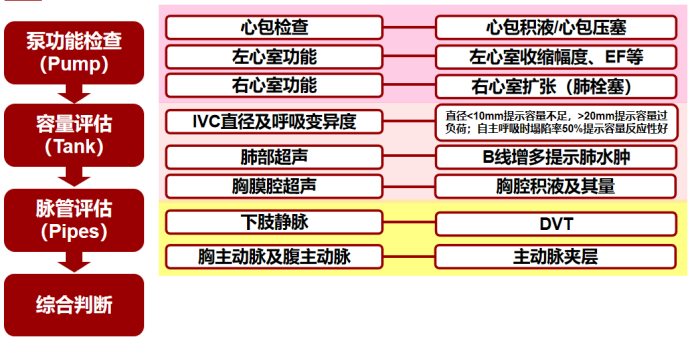
图18 RUSH方案
床旁超声凭借可靠、可重复的特性,成为临床诊疗的得力工具。它能精准捕捉关键生理参数与病因信息,通过定量与定性结合,辅助识别严重的情况以及指导合适的治疗(如补液方案调整),且操作快速安全、适配急重症救治节奏。但该技术也存在一定的局限,例如超声图像质量易受患者体型、肺部气体干扰,诊断依赖操作者技能,复杂病理状态(如多器官衰竭)下需结合血流动力学监测、实验室检查等,协同实现精准诊疗。
致谢:感谢北京大学第三医院心血管内科李丹教授提供的部分珍贵图片及视频资料。
作者介绍

梁瀛
北京大学第三医院呼吸与危重症医学科副主任,医学博士,主任医师,副教授,硕士生导师;中华医学会呼吸病学分会慢阻肺学组委员,中国老年医学学会呼吸病学分会呼吸生理与肺功能学组委员,北京医学会呼吸病学分会慢阻肺学组委员兼工作秘书,北京慢性病防治与健康教育研究会呼吸专业委员会委员,北京防痨协会第十二届理事会理事,北京大学医学部慢性气道疾病研究中心工作秘书,北京市慢性肺部疾病学术联盟专家委员会常委。
本文仅用于学术内容的探讨和交流,不用于任何商业和推广,亦不作为最终的临床决策。临床实践需根据患者的具体情况选择适宜的处理措施。
 后可发表评论
后可发表评论

相关推荐
1
肺活检(支气管镜操作)所致大出血的预防与救治
1.2w
2
詹庆元教授:重症肺炎的救治:如何降低病死率?
1.1w
3
李琦教授:重症肺炎早期诊断和危险分层生物标志物研究进展
8631
4
床旁支气管镜在RICU/MICU中的介入治疗
7805
5
一次性支气管镜在RICU有必要吗?
6952
6
健康中国 春归武汉|解立新教授专访:M-ROSE在ICU患者肺部真菌感染中的应用
6563
7
俯卧位通气在重症肺炎中的应用进展
6559
8
黎毅敏教授:重症肺炎的诊治——来自AI的视角
6034
9
通过内标分子进行人源/病原核酸定量宏基因组测序与肺炎诊断
5960
10
重症肺部感染病原学诊断的巨大进步:浅谈二代测序技术
5848



友情链接
联系我们
 公众号
公众号
 客服微信
客服微信